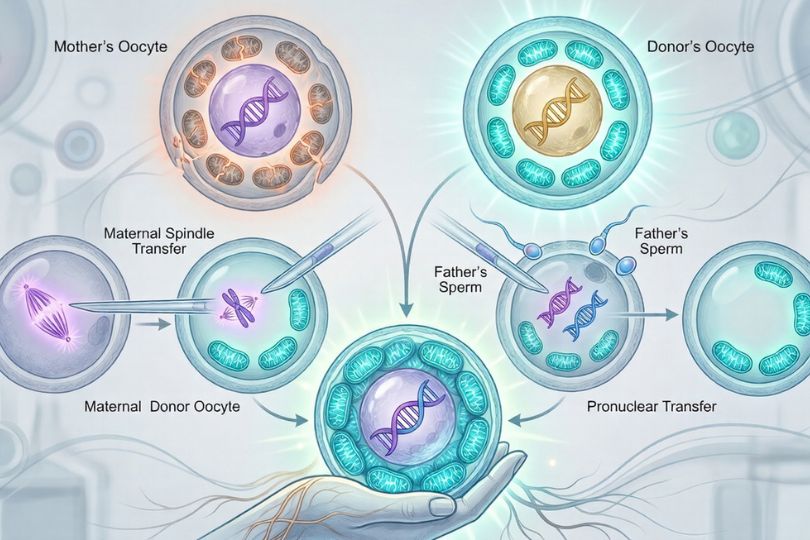
Новейшие инновации во вспомогательных репродуктивных технологиях (ВРТ)

Вспомогательные репродуктивные технологии (ВРТ) очень быстро меняются: если раньше главным вопросом было «сделать ЭКО», то сегодня фокус — как точнее выбрать эмбрион, как повысить имплантацию, как снизить инвазивность и как помочь тем, у кого нет собственных гамет или матки.
Ниже — самые актуальные направления, включая технологии, которые ещё находятся на этапе исследований.
- ИИ + таймлапс-эмбриология: «умный» отбор эмбрионов
Что это: эмбрионы выращивают в инкубаторах с камерой (time-lapse), которые постоянно снимают развитие. Далее алгоритмы (deep learning) анализируют морфокинетику и прогнозируют потенциал имплантации/беременности.
Почему это важно:
- меньше субъективности (разные эмбриологи могут оценивать по-разному);
- больше данных: не один «кадр», а весь «фильм» развития;
- перспектива персонализированных решений (с учётом возраста, истории, протокола и т.д.).
Где сейчас граница: эффективность ИИ зависит от качества датасетов, стандартизации лабораторий и внешней валидации. Есть много обзоров и моделей, но клинические доказательства «везде и для всех» ещё накапливаются.
- Неинвазивное генетическое тестирование эмбриона (niPGT-A): без биопсии
Что это: вместо биопсии трофэктодермы (когда берут клетки эмбриона) анализируют cell-free DNA в среде культивирования («spent culture media»). Идея — сделать оценку хромосомных нарушений менее травматичной.
Почему это «вау»: потенциально меньше инвазивности, проще логистика, возможно — более широкий доступ в будущем.
Но важно: тема очень дискуссионная, потому что ключевые проблемы — смешивание эмбриональной и материнской ДНК, низкое количество ДНК, риск ложных результатов. Есть работы, которые подчёркивают «серьёзные вызовы точности», поэтому сейчас это скорее перспективное направление или «backup/дополнительный инструмент», а не полная замена стандартного PGT-A.
- «Модель эндометрия в лаборатории»: прорыв в изучении имплантации
Одна из самых сложных стадий — имплантация. И долгое время её было трудно изучать напрямую.
Недавно исследователи сообщили о создании лабораторного аналога слизистой матки (эндометрия), в который смогли имплантировать ранние эмбрионы (в рамках этических ограничений исследований). Это открывает путь к лучшему пониманию причин неудач имплантации и потенциально — к новым подходам в лечении.
- Трансплантация матки (UTx): от «эксперимента» к реальному лечению для отдельных случаев
Для кого: женщины с абсолютным маточным фактором бесплодия (отсутствие матки, тяжёлые врождённые синдромы, удаление матки и т.д.).
Сегодня UTx уже имеет десятки рождений в мире и рассматривается как жизнеспособный вариант лечения в специализированных центрах (несмотря на сложность операции и необходимость иммуносупрессии).
- In vitro gametogenesis (IVG): «яйцеклетки/сперматозоиды из клеток кожи» — пока что преимущественно уровень науки
Что это: попытки получить гаметы из плюрипотентных стволовых клеток (iPSC). Это могло бы помочь людям, которые не имеют собственных гамет (например, после онколечения), и в будущем — расширить возможности для различных семейных ситуаций.
Статус: для человека это пока что очень ранний этап, с большими биологическими и этическими вызовами. Есть обзоры и экспериментальные работы, которые объясняют потенциал и сложность переноса результатов с животных моделей на человека.
Отдельно в 2025 году появились громкие новости о создании «яйцеподобных» клеток из клеток кожи и ранних экспериментах с оплодотворением — но авторы и независимые эксперты подчёркивают: до клиники ещё очень далеко.
- «Умные» стратегии повышения шансов имплантации: персонализация вместо «одного стандарта для всех»
Параллельно с «большими прорывами» идут практические инновации:
- более точные алгоритмы ведения стимуляции;
- подбор тактики переноса (fresh/frozen, одиночный перенос);
- интеграция больших данных (эмбриология + клиника + генетика) для персонализации.
В этом направлении ключевую роль как раз и играют ИИ-подходы и стандартизация лаборатории.
Что из этого «самое новое» именно сейчас
Если коротко по уровню готовности:
Уже активно в клиниках:
- time-lapse мониторинг (во многих центрах) + постепенное внедрение ИИ-оценки;
- расширение показаний и протоколов, больше персонализации.
На границе клиники / в активных исследованиях:
- неинвазивное PGT-A (много работ, но точность и стандарты ещё «болят»).
Преимущественно исследования / proof-of-concept:
- лабораторные модели эндометрия для изучения имплантации;
- IVG / «гаметы из iPSC», «яйцеклетки из кожи» — пока что очень далеко от рутины.
Медицинский центр BioTexCom уже сегодня внедряет часть самых современных достижений вспомогательных репродуктивных технологий, чтобы повысить эффективность программ суррогатного материнства и донорства яйцеклеток. В работе используются усовершенствованные эмбриологические протоколы, современные методы культивирования эмбрионов, персонализированный подбор тактики лечения и строгий лабораторный контроль на каждом этапе. Сочетание инноваций, многолетнего опыта команды и комплексного медико-юридического сопровождения позволяет BioTexCom стабильно улучшать результаты и помогать семьям со всего мира становиться родителями.