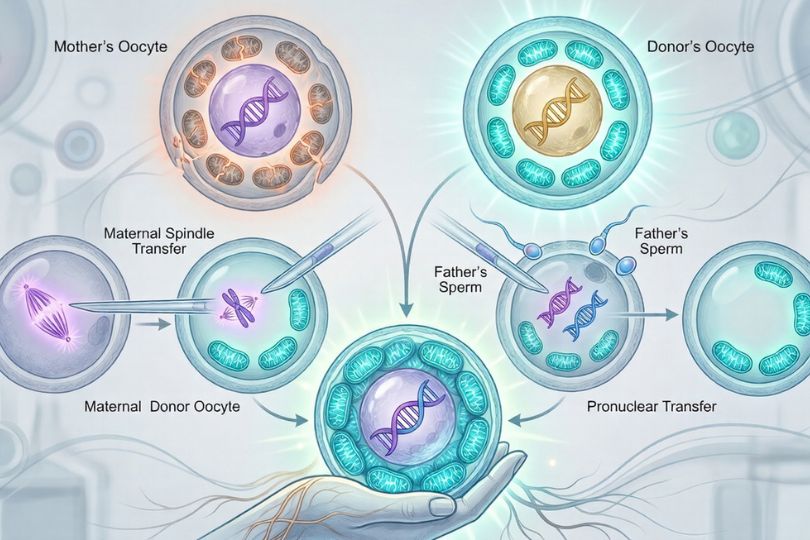
Найновіші інновації в допоміжних репродуктивних технологіях (ДРТ)

Допоміжні репродуктивні технології (ДРТ) дуже швидко змінюються: якщо раніше головним питанням було “зробити ЕКЗ”, то сьогодні фокус — як точніше вибрати ембріон, як підвищити імплантацію, як зменшити інвазивність і як допомогти тим, у кого немає власних гамет або матки.
Нижче — найактуальніші напрями, включно з технологіями, які ще на етапі досліджень.
- ШІ + таймлапс-ембріологія: «розумний» відбір ембріонів
Що це: ембріони вирощують у інкубаторах із камерою (time-lapse), які постійно знімають розвиток. Далі алгоритми (deep learning) аналізують морфокінетику й прогнозують потенціал імплантації/вагітності.
Чому це важливо:
- менше суб’єктивності (різні ембріологи можуть оцінювати по-різному);
- більше даних: не один “кадр”, а весь “фільм” розвитку;
- перспектива персоналізованих рішень (з урахуванням віку, історії, протоколу тощо).
Де зараз межа: ефективність ШІ залежить від якості датасетів, стандартизації лабораторій і зовнішньої валідації. Є багато оглядів і моделей, але клінічні докази «всюди і для всіх» ще накопичуються.
- Неінвазивне генетичне тестування ембріона (niPGT-A): без біопсії
Що це: замість біопсії трофектодерми (коли беруть клітини ембріона) аналізують cell-free DNA у середовищі культивування (“spent culture media”). Ідея — зробити оцінку хромосомних порушень менш травматичною.
Чому це «вау»: потенційно менше інвазивності, простіша логістика, можливо — ширший доступ у майбутньому.
Але важливо: тема дуже дискусійна, бо ключові проблеми — змішування ембріональної та материнської ДНК, низька кількість ДНК, ризик хибних результатів. Є роботи, що підкреслюють “серйозні виклики точності”, тому зараз це скоріше перспективний напрям або “backup/додатковий інструмент”, а не повна заміна стандартного PGT-A.
- «Модель ендометрію в лабораторії»: прорив у вивченні імплантації
Одна з найскладніших стадій — імплантація. І довгий час її було важко вивчати напряму.
Нещодавно дослідники повідомили про створення лабораторного аналога слизової матки (ендометрію), у який змогли імплантувати ранні ембріони (в межах етичних обмежень досліджень). Це відкриває шлях до кращого розуміння причин невдач імплантації та потенційно — до нових підходів у лікуванні.
- Трансплантація матки (UTx): від «експерименту» до реального лікування для окремих випадків
Для кого: жінки з абсолютним матковим фактором безпліддя (відсутність матки, важкі вроджені синдроми, видалення матки тощо).
Сьогодні UTx вже має десятки народжень у світі й розглядається як життєздатний варіант лікування у спеціалізованих центрах (попри складність операції та необхідність імуносупресії).
- In vitro gametogenesis (IVG): “яйцеклітини/сперматозоїди з клітин шкіри” — поки що переважно рівень науки
Що це: спроби отримати гамети з плюрипотентних стовбурових клітин (iPSC). Це могло б допомогти людям, які не мають власних гамет (наприклад, після онколікування), і в майбутньому — розширити можливості для різних сімейних ситуацій.
Статус: для людини це поки що дуже ранній етап, з великими біологічними й етичними викликами. Є огляди та експериментальні роботи, які пояснюють потенціал і складність перенесення результатів із тваринних моделей на людину.
Окремо в 2025 році з’явилися гучні новини про створення “яйцеподібних” клітин із клітин шкіри та ранні експерименти з заплідненням — але автори й незалежні експерти наголошують: до клініки ще дуже далеко.
- «Розумні» стратегії підвищення шансів імплантації: персоналізація замість “одного стандарту для всіх”
Паралельно з “великими проривами” йдуть практичні інновації:
- точніші алгоритми ведення стимуляції;
- підбір тактики перенесення (fresh/frozen, одиночний перенос);
- інтеграція великих даних (ембріологія + клініка + генетика) для персоналізації.
У цьому напрямі ключову роль якраз і грають ШІ-підходи та стандартизація лабораторії.
Що з цього “найновіше” саме зараз
Якщо коротко за рівнем готовності:
Вже активно в клініках:
- time-lapse моніторинг (у багатьох центрах) + поступове впровадження ШІ-оцінки;
- розширення показань і протоколів, більше персоналізації.
На межі клініки / в активних дослідженнях:
- неінвазивне PGT-A (багато робіт, але точність і стандарти ще “болять”).
Переважно дослідження / proof-of-concept:
- лабораторні моделі ендометрію для вивчення імплантації;
- IVG / “гамети з iPSC”, “яйцеклітини зі шкіри” — поки що дуже далеко від рутини.
Медичний центр BioTexCom уже сьогодні впроваджує частину найсучасніших досягнень допоміжних репродуктивних технологій, щоб підвищити ефективність програм сурогатного материнства та донації яйцеклітин. У роботі використовуються вдосконалені ембріологічні протоколи, сучасні методи культивування ембріонів, персоналізований підбір тактики лікування та суворий лабораторний контроль на кожному етапі. Поєднання інновацій, багаторічного досвіду команди та комплексного медико-юридичного супроводу дозволяє BioTexCom стабільно покращувати результати та допомагати сім’ям з усього світу ставати батьками.